رفرنس استاندارد دارویی USP + استاندارد دارویی آمریکا
استاندارد دارویی ایالات متحده (USP) به عنوان یک مرجع برجسته جهانی در زمینهی کیفیت دارویی، در طول سال ها نقش مهمی در تضمین ایمنی و کارایی محصولات دارویی ایفا کرده است. USP که مخفف عبارت "United States Pharmacopeia" می باشد، سازمانی است که با هدف تدوین استاندارد ها و معیار های کیفیت برای دارو ها، مکمل های غذایی و مواد زیستی تأسیس شده است. این سازمان از سال 1820 فعالیت خود را آغاز کرده و امروزه به یکی از معتبر ترین مراجع در سطح جهان تبدیل شده است. استاندارد دارویی USP نه تنها برای تولید کنندگان دارویی، بلکه برای محققان، ناظران و حتی مصرف کنندگان عادی نیز اهمیت بسیاری دارد. در این مقاله، به بررسی جامع و دقیق استاندارد دارویی USP خواهیم پرداخت و ابعاد مختلف آن را از جمله تاریخچه، اهمیت، فرآیند های تدوین استاندارد ها و کاربرد های آن در صنایع مختلف بررسی خواهیم کرد.




















بررسی تاریخچه رفرنس استاندارد دارویی usp

مزایای استفاده از استاندارد دارویی USP
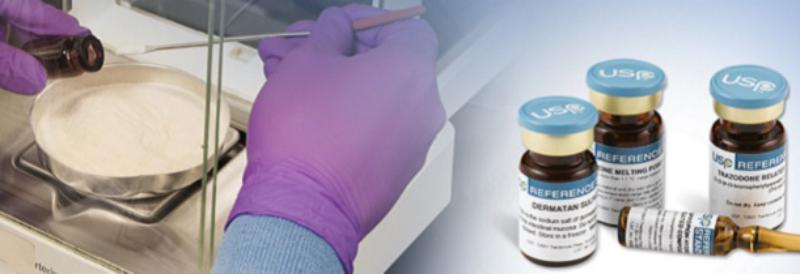
بررسی استاندارد های مرجع

بررسی استاندارد های مستند

استاندارد دارویی USP چیست؟
USP شامل چه مواردی می باشد؟

شیوه ی ایجاد استاندارد دارویی USP

نقش و اهمیت USP در صنعت داروسازی
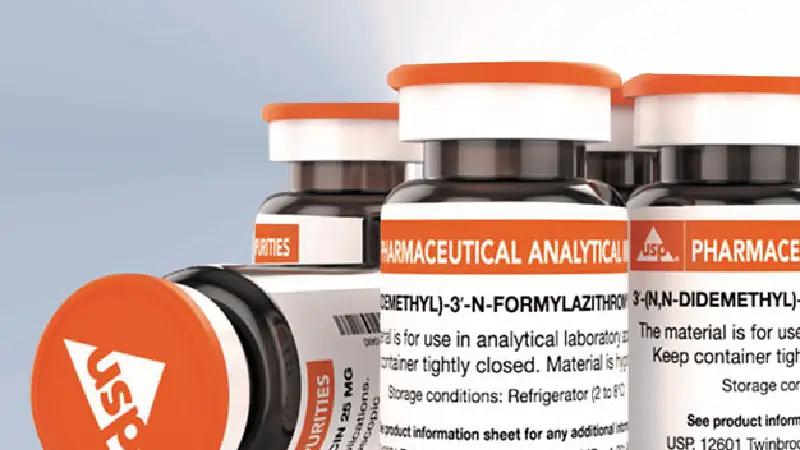
فرآیند تدوین استاندارد های USP
کاربرد های USP در صنایع مختلف
نقش USP در بهبود سلامت عمومی
بررسی چالش های پیش روی USP

آدرس: تهران ، اتوبان چمران جنوب - نرسیده به میدان توحید- باقرخان غربی -پلاک ۱۰۱ - واحد ۳
شما میتوانید با تماس با کارشناسان ایمن گستر شیمی از مشاوره رایگان استفاده کرده و ما به صورت کامل پاسخگوی سوالات شما عزیزان هستیم ، همچنین اگر کالای خاصی مد نظر شما باشد در تهیه آن شما را راهنمایی کنیم .